Me he quedado como el profesor del colegio de «Amanece que no es poco», cuando me han dicho que no hay que hacer las pruebas de Bowie-Dick y que podía valer con los biológicos. Un biológico no sustituye al Bowie y viceversa.
Eso si, le he dicho que debe poner los indicadores biológicos semanales, que se deben leer a las 48 horas y además usar un testigo o control. Hagamos repaso a lo que dicen las Guías como la del Hospital Universitario de Ceuta.
Durante los años 50, varios expertos del campo de la tecnología de esterilización de cargas porosas detectaron graves defectos en la forma en que los esterilizadores de los hospitales se estaban utilizando en el Reino Unido. A raíz de estos informes, muchos profesionales empezaron a desarrollar un medio para someter a pruebas dichos esterilizadores de forma rápida, sencilla y, lo más importante, económica. Estos esfuerzos culminaron con la publicación de una serie de estudios de J.H. Bowie. Su escrito más conocido es el publicado en Lancet. En el Reino Unido, el Ministerio de Sanidad británico (HTM0106_PartA) adoptó este test y lo incluyó en el Memorando Técnico de Sanidad número 10 como prueba de funcionamiento diaria para esterilizadores de carga porosa, desde entonces es una prueba de obligado cumplimiento y de realización diaria (UNE-EN-ISO 17665: 2007).

La prueba o control de Bowie-Dick es un test de desafío que se diseña para constituir una resistencia definida a una proceso de esterilización y utilizados para evaluar el funcionamiento del proceso (apartado 3.34 y 12.1.6 de la UNE-EN-ISO 17665-1), están construidos de manera que pueden alojar en su interior un sistema de indicador químico o biológico en una posición que hace difícil la entrada del agente esterilizante. Pueden ser de dos tipos, por un lado tenemos las pruebas para cargas porosas como la prueba de Bowie-Dick, y por otro lado están los dispositivos de carga hueca (Hollow load); mal llamado Test Hélix que proviene de la Hélice de Pickerill-Line.
El Control Bowie-Dick es un control de los equipos de vapor con vacío (B y S), es decir, no vale en el caso de los miniclaves de tipo N (más información en esta entrada de los miniclaves y la de esterilización en primaria. El Test Bowie-Dick es una prueba de obligado cumplimiento y de realización diaria en grandes esterilizadores (UNE-EN-ISO 17665: 2007); en los esterilizadores pequeños se recomienda el Test Hélix (EN 867-5), debido a los posibles errores de penetración del Bowie-Dick, aunque se pueden usar.
La esterilización se consigue mediante la penetración rápida y uniforme de vapor en todas las partes de la carga del autoclave, siendo fundamental eliminar el aire de la cámara y de la carga y aplicar un suministro de vapor que contenga un volumen mínimo de gases no condensables. El Test Bowie-Dick revela si la penetración del vapor en el paquete de prueba ha sido rápida y uniforme.
Mediante la prueba de Bowie-Dick, que es un indicador de clase 2, se controla que el vacío se haya realizado correctamente y que el vapor haya penetrado totalmente. De este modo nos indicará que el equipo esta preparado para esterilizar. Se efectuará en el primer programa del día, después del programa de precalentamiento. Debe hacerse también, siempre después de cualquier reparación. Ningún otro dispositivo sustituirá al Bowie-Dick (Web del Hospital de Ciudad Real, España).
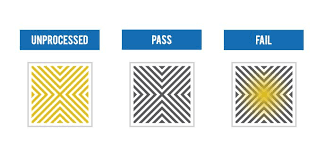
Todas las hojas de prueba del Test Bowie-Dick están impresas con una tinta que cambia de color, normalmente de blanco a negro. El cambio de color depende de la presencia de humedad y una elevada temperatura. Deben darse ambos factores para que se produzca el cambio de color en un período de tiempo muy corto (período de exposición de 3,5 minutos o 210±5 segundos en el período meseta) a 132-134ºC. Existe un programa específico en estos miniclaves para la realización del test y se utilizan paquetes comerciales de un solo uso. Se usará un solo paquete de prueba, sin otra carga adicional, en posición horizontal en la zona anteroinferior de la cámara, cerca de la puerta y sobre el desagüe.

El Test Bowie-Dick emplea indicadores químicos de Clase B que se ajustan a la norma UNE-EN 867-3 (apartado 7.38) o UNE-EN-ISO 11140-1: 2007 que lo clasifica como de tipo 2. La UNE-EN-ISO 17665-2: 2009 da la recomendación de realizar diariamente la Prueba de Bowie-Dick y la Prueba de “carga hueca tipo A” anualmente, que está definida en la UNE-EN 13060.
Un resultado inicial no satisfactorio obliga a realizar una segunda prueba, y si ésta vuelve a ser incorrecta, esto indica que el esterilizador de vapor no funciona correctamente, por lo que no debe utilizarse hasta que se haya solucionado el fallo o avería.
Cuadro Resumen del Control de calidad para la esterilización por vapor
| CONTROL | TIPO | FRECUENCIA |
|
FISICO |
Presión
Temperatura Tiempo |
Por ciclo
Por ciclo Por ciclo |
| PRUEBA DE VACIO | Bowie-Dick | Diario |
| QUIMICO | Interno
Externo |
Paquete > 30 L.
Todos los paquetes |
| BIOLOGICO | Esporas de Geobacillus stearothermophilus | Semanal |
Hay dispositivos de desafío helicoidal (el hélix) que podrán usarse como complementarios, pero nunca sustituir al Bowie-Dick, excepto en los miniclaves, para los que sí están indicados. Para esterilizadores pequeños (UNE-EN 13060: 2005+ AC1 2007+ AC2 2009) se recomienda el desafío de tipo hélice o Test Hélix (EN 867-5) en lugar del Bowie-Dick de forma diaria; aunque éstos últimos se pueden utilizar en el ciclo correspondiente de 3,5 minutos a 132-134ºC.
Además del test de desafío, tenemos el test de penetración. Para comprobar la correcta extracción del aire y el proceso de penetración del vapor (Test de penetración), se utiliza un dispositivo de prueba (Hélix, de acuerdo con EN- 13060-2 y EN 867-5) y es obligatorio en los equipos S y B.
Para los «manitas» y con tiempo, el paquete de prueba Bowie-Dick se puede preparar siguiendo las directrices de la AAMI o utilizar paquetes semi o desechables, que demuestren su equivalencia, y que es lo más frecuentemente utilizado. El paquete para la prueba Bowie-Dick de la AAMI consiste de:
- Toallas de algodón 100%, recién lavadas (sin planchar). El número depende del espesor y del uso de las toallas.
- Material de empaquetado de tela o tejido no tejido.
Las toallas deben doblarse hasta un tamaño no menor de 23 cm. en una dirección y 30 cm. en la otra dirección, y colocadas una sobre otra. La altura del paquete debe ser de 25 a 28 cm. Se coloca la hoja indicadora de prueba se coloca en el centro del paquete, y después se envuelve con una envoltura de tejido sin tejer. Los paquetes de Bowie-Dick semi- o desechables reducen el riesgo de error y aseguran un funcionamiento uniforme y deben seguir el mismo procedimiento de colocación e interpretación que el paquete de prueba de la AAMI (25). En las Normas UNE-EN 867-4 y UNE-EN-ISO 11140-3: 2007+ AC 2009 se especifican los requisitos de funcionamiento de los paquetes de prueba alternativos para su uso en el Test Bowie-Dick y que, asimismo, parte de que demuestren un rendimiento equivalente al del paquete de toallas estándar.
Es importante saber que hay tres tipos diferentes de pruebas o versiones de Bowie-Dick que debemos conocer y tener en cuenta en el momento de su uso. La norma UNE-EN 285: 2007+ AC1 2008+ AC2 2009 y el estándar americano AAMI/ANSI ST79 describen :
– Versión americana (ISO 11140-5) que simula un paquete de prueba de algodón de 4 Kg. ± 200 gr. (± 5%) en un paquete de 24x35x29 cm. y que denominan DART (Daily Air Removal Test) para ciclos de 132º C durante 3 minutos. Se ajusta a los estándares de la AAMI/ANSI ST79.
– Versión europea (UNE-EN-ISO 11140-4: 2007) que cumple con la UNE-EN 285 (apartado 17) y se valida para un paquete de 7 Kg. ± 10%, de 25x35x20 cm., en un programa de 134º C durante 3,5 minutos o 121º C en 15 minutos. Vemos que es diferente y superior en peso al paquete americano, por lo que es más sensible.
– Versión europea (UNE-EN-ISO 11140-4: 2007 y UNE-EN 867-5:2002) para paquetes de 7 Kg. y que cumple los test de carga hueca, que requiere adicionalmente la norma 285, y la UNE-EN 13060 para los miniclaves de tipo B y S.
En los últimos años se han desarrollado dispositivos electrónicos alternativos para realizar la prueba de Bowie-Dick, ofreciendo un registro electrónico, además de múltiples funciones diagnósticas. El Sistema de Prueba Electrónico o Electronic Test System (SPE® en castellano o ETS® en inglés) de 3M® realiza una verificación electrónica única, cuya finalidad es satisfacer las necesidades actuales de normativa, así como la necesidad de mejorar la calidad y la productividad al tiempo que se reducen errores y por lo tanto costes (12). A diferencia de cualquier otro sistema de prueba, el SPE® es un dispositivo especial que funciona como dispositivo de medida independiente y que proporciona claros resultados de “Apto” o “No Apto” y de “Advertencia Previa” de la Prueba de Bowie-Dick (14). También indica si se han alcanzado los parámetros de esterilización específicos (p.ej., 134º C a 3,1 atmósferas de presión absoluta, durante 3,5 minutos en la meseta). Los resultados son reproducibles y equivalentes en rendimiento a un paquete de prueba Bowie- Dick estándar, para satisfacer los requisitos diarios de comprobación de la penetración del vapor detallados en la Norma UNE-EN 554. El Software también genera mediciones para la Prueba de la Tasa de Fuga (según la Norma UNE-EN 285), el cálculo de la F0 y una indicación de parámetros de esterilización. El sistema de Prueba electrónico para esterilizadores de vapor por prevacío es un dispositivo analítico electrónico fácil de utilizar, que proporciona una información amplia, objetiva e independiente acerca de las variables críticas del proceso de esterilización por vapor. El dispositivo mide la temperatura, el tiempo, la presión y aire residual. El SPE® está avalado por un organismo de certificación externo a 3M® (como así exige la normativa), que lo testa de acuerdo a los requisitos de la UNE-EN 285 y UNE-EN-ISO 11140-4 (12,13,25).
Otros sistemas similares y con las mismas prestaciones son el Interster Digital Helix System® de Interster® y el Wi Scan® System de Sterlab® en cuanto a cumplimiento de normativas internacionales, mediciones, vida útil y usos (400-500 usos). Este último sistema permite además introducir la sonda de medida dentro de un contenedor de instrumental reflejando por tanto las condiciones a las que es sometido el instrumental.
Lo sé, me ha quedado una entrada larga, pero es que…

Normativa relacionada con la prueba de Bowie-Dick:
UNE EN ISO 11140-3:2009 Sistemas no biológicos para uso en esterilizadores. Parte 3: especificaciones para los indicadores de clase B para uso en el ensayo de Bowie y Dick.
UNE-EN ISO 11140-4:2007 Sistemas no biológicos para uso en esterilizadores. Parte 4: especificación para los indicadores como alternativa al ensayo de Bowie y Dick para la detección de la penetración del vapor.
Este es otro Bowie (El gran Duque Blanco)


















































Debe estar conectado para enviar un comentario.