🔍 Un nuevo informe del Grupo de Expertos en Evaluación del Desempeño de los Sistemas de Salud (HSPA) de la Comisión Europea destaca la urgente necesidad de identificar, medir y reducir las prácticas sanitarias que no aportan valor real a los pacientes🏥💸. El informe, publicado en febrero de 2025, se basa en una revisión bibliográfica del estado de la cuestión y en los resultados de una encuesta realizada por el grupo de expertos en HSPA (si conseguís saber quiénes son los expertos, me lo decís, no consigo encontrarlos).
🚫 Estas intervenciones, conocidas como «low-value care», pueden:
❌ No tener beneficios clínicos
⚠️ Generar daño
💰 Malgastar recursos
🌍 Afectar negativamente al medio ambiente
El informe propone una definición amplia e innovadora que incluye:
– Uso excesivo/inapropiado (ej: pruebas innecesarias)
– Uso insuficiente (ej: falta de servicios necesarios)
– Variaciones injustificadas (ej: diferencias entre regiones sin razón médica)
El grupo de expertos de la Comisión Europea establece un nuevo marco conceptual con nueve definiciones o tipos de prácticas de bajo valor (PBV), clasificadas en tres grandes categorías:
– Uso excesivo o inapropiado (5 tipos de PBV): incluye intervenciones sin beneficio demostrado y aquellas con alternativas más costo-efectivas o que se realizan en niveles asistenciales innecesariamente costosos.
– Uso insuficiente (2 tipos de PBV): se refiere a servicios necesarios que no se ofrecen o no se utilizan, lo que compromete los resultados en salud.
– Variaciones injustificadas (2 tipos de PBV): son las diferencias geográficas o entre grupos poblacionales que no se explican por necesidades clínicas y que pueden reflejar tanto sobreutilización como infrautilización.

Ejemplos de prácticas de bajo valor:
💊 Uso excesivo de antibióticos
🦴 Radiografías tempranas sin necesidad
🧴 Niveles de vitamina D en personas sanas
👵 Medicación inapropiada en mayores
🏥 Hospitalizaciones evitables
📌 Recomendaciones clave:
📚 Guiarse por evidencia y crear herramientas de decisión.
🏗️ Reorganizar servicios.
📈 Medir resultados y dar retroalimentación.
📣 Informar y sensibilizar a pacientes y profesionales.
🌱 Ampliar el concepto de “valor”: salud, equidad y sostenibilidad.
🌍 Ejemplo inspirador en España es la iniciativa “No Hacer”.
La reducción de prácticas de atención de bajo valor no solo optimiza la eficiencia del sistema de salud y minimiza el riesgo de daño evitable en los pacientes, sino que también constituye una oportunidad estratégica para reorientar recursos hacia intervenciones de alto valor. Esta transición favorece la equidad en el acceso, disminuye la huella ambiental del sistema sanitario y contribuye a su sostenibilidad a largo plazo. La integración de su medición en los procesos de evaluación del desempeño es esencial para consolidar un modelo de atención verdaderamente orientado al valor.
✅ Reducir la atención de bajo valor = + salud + equidad + eficiencia + sostenibilidad
¡Una prioridad para los sistemas sanitarios del futuro! 🚀🌿
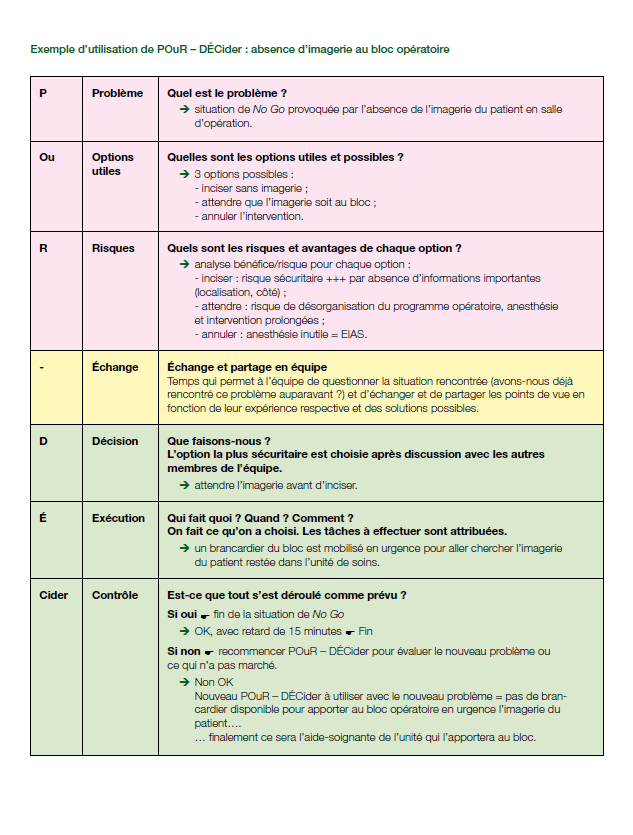
Pues todo esto viene a raíz de una de las categorías. En concreto, es una denominada de la categoría “Uso excesivo o inapropiado”, que incluye intervenciones más costoefectivas o sostenibles. Pues aparece con la letra D, que es el “Uso de material médico único cuando se podría reutilizar en múltiples usos”, y he buscado el original en el Informe (página 17 y 20):

“Single-use medical material that could be sterilised for multiple use”, que puede traducirse como “Material médico de un solo uso que podría esterilizarse para usos múltiples”. Y este es un tema del que hemos hablado y discutido demasiado en este Blog. Los dispositivos de un solo uso son de un solo uso, y no se pueden reesterilizar porque lo prohíbe la normativa vigente (Real Decreto 192/2023) y para mantener la seguridad de nuestros pacientes.
Creo que lo correcto sería escribir: Es preferible utilizar material médico reutilizable seguro, en lugar de productos de un solo uso.

https://doi.org/10.1016/S0140-6736(25)01099-2
Aprovecho para traeros este artículo de Kremer (Sobieski, W., Kremer, T., Tortora, A., Rodriguez, C., Rauber, J., Znamensky, D., Todd, A., & McDonnell, G. (2025). Processing Reusable Medical Devices and End-of-Life Investigation. Biomedical instrumentation & technology, 59(2), 136–144. https://doi.org/10.2345/0899-8205-59.2.136), que no lo puedo poner en abierto. Que viene a decirnos que los productos sanitarios reutilizables están destinados a ser sometidos a múltiples ciclos de procesamiento clínico a lo largo de su vida útil, de conformidad con las instrucciones de uso del fabricante (IFU). De ahí la importancia económica y medioambiental de utilizar productos reutilizables y no de un solo uso. Las IFU deben incluir información práctica sobre la vida útil del producto sanitario. En este estudio de Kremer de laboratorio se investigó un enfoque para respaldar una vida útil indefinida de los dispositivos reutilizables (¡obsolescencia programada en la central!), en el que el final de la vida útil depende de la inspección visual y la verificación funcional proporcionadas en las IFU. Los dispositivos se sometieron a ciclos repetitivos de procesamiento (limpieza, desinfección y esterilización). En distintas fases del estudio, se examinaron los defectos visuales de los dispositivos a lo largo del tiempo. Además, se evaluaron los niveles extraídos de carbono orgánico total y citotoxicidad.
Los resultados indicaron que los efectos de los ciclos repetidos de procesado en el dispositivo ensayado fueron insignificantes en cuanto a daños físicos y niveles químicos residuales. Estos resultados apoyan una vida útil indefinida del dispositivo utilizando las indicaciones de fin de vida útil, basadas en la IFU y los requisitos de inspección (limpieza, daños y funcionamiento correcto).
De este artículo (George RE, Bay CC, Shaffrey EC, Wirth PJ, Rao VK. A Day in the Life of a Surgical Instrument: The Cycle of Sterilization. Ann Surg Open. 2024 Feb 22;5(1):e381. doi: 10.1097/AS9.0000000000000381. PMID: 38883953; PMCID: PMC11175864) se obtienen algunas conclusiones:
- El costo de esterilización por instrumento varía entre USD $0.59 y $11.52.
- Sólo se utiliza entre el 13% y el 22% de los instrumentos incluidos en bandejas estándar.
- La vida útil típica de un instrumento oscila entre 300 y 900 ciclos de esterilización, aunque no suele llevarse un registro individual.
- Optimizar el tamaño de las bandejas puede reducir hasta un 70% la esterilización innecesaria, ahorrando millones de dólares anuales sin afectar los tiempos quirúrgicos.
- Con un mejor diseño de bandejas, registro de ciclos y conciencia del personal quirúrgico, es posible aumentar la eficiencia, prolongar la vida útil de los instrumentos y reducir gastos sin comprometer la calidad asistencial.
- Reducción del procesamiento redundante para aumentar la vida útil de los instrumentos y disminuir costos.
- El proceso de esterilización quirúrgica es complejo, esencial para la seguridad y con un fuerte impacto económico.
Entrada realizada con la ayuda de: https://sano-y-salvo.blogspot.com/2025/08/la-identificacion-medicion-y-reduccion.html?m=1&s=09
La Sociedad Española de Desinfección y Esterilización (SEDE) lanza un nuevo episodio de su espacio “SEDE Opina”, un podcast dedicado a compartir conocimiento, experiencias y buenas prácticas sobre desinfección, esterilización y prevención de infecciones relacionadas con la asistencia sanitaria.
En este formato ágil y cercano, nuestros especialistas analizan los retos actuales en la seguridad del paciente, la gestión de centrales de esterilización y la implantación de normas internacionales (ISO 13485, ISO 17665, ISO 15883) en los entornos hospitalarios.
🎧 Escúchalo aquí: https://lnkd.in/dbTrzKrM
🔗 Descubre cómo la innovación y la formación continua fortalecen la calidad asistencial.
Ya sé que esta entrada no es de las habituales de esterilización, con sus Bowie-Dick o los sistemas de envasado, pero creo que la profesionalización de las centrales pasa por incluir más temas de gestión.
Aunque para presentar alimentos, nadie mejor que Lolo Torosio, qué arte presentando unos huevos fritos con pisto o unos churros. Dan ganas de comérselos.
Y después de ponernos bien de comer, un poco de leche de coco. Casi me da vergüenza ajena ver el vídeo. No hay desperdicio por ningún sitio: los bailarines con pelo en pecho, la bailarina con esa especie de moño y el solista al más puro Demis Roussos.

Enlace: https://forms.office.com/e/86XFaF2kEv

El “Máster en Reprocesamiento de productos sanitarios” permitirá a los profesionales que dirijan Centrales de Esterilización que profundicen su formación a través de la adquisición de un avanzado nivel de conocimientos teóricos, técnicos y metodológicos en el área del reprocesamiento de productos sanitarios; brindándoles las herramientas científicas y prácticas para desarrollarse como especialistas en éste ámbito.
El programa está dividido en 3 módulos, cada uno de los cuales incluye una parte de formación y una parte de evaluación.
Los módulos deberán consultarse en el orden predeterminado, y sólo se podrá avanzar al siguiente módulo si la evaluación del módulo anterior es satisfactoria.
El Máster es totalmente online, tiene una duración de 10 meses y el coste total es de 2.250 euros.
Recuerda que las plazas son limitadas.
Para obtener más información o resolver tus dudas sobre el máster, puedes contactar con masterrpseuneiz@gmail.com o llamando al teléfono de la Universidad de Vitoria-Gasteiz (EUNEIZ): +34 637 844 471.
¡Esperamos verte en el Máster!























































Debe estar conectado para enviar un comentario.