Vuelvo a rescatar una entrada del blog de la empresa Matachana. Esta vez es sobre el tratamiento del instrumental de laparoscopia, y en concreto las ópticas.

Lo primero que debemos ver es si nuestro material es resistente al vapor de agua. ¿Y cómo lo sabemos? Pues buscando las instrucciones del fabricante (IFU) o viendo el color de una zona de la óptica, que si es de color marrón suele ser esterilizable mediante vapor de agua, y con otros colores, pues será con sistemas de esterilización en frío. Son muchos los que insisten en que la esterilización con el vapor de agua disminuye la vida media de las ópticas o las estropea más; aunque lo más aconsejable es seguir las recomendaciones del fabricante.
Y cuidado con los baños de ultrasonidos que las deterioran; no atribuyamos todos los males al vapor de agua (página 95).
Y aquí viene la pregunta, si decidimos hacerlo en frío, deberemos decidir si lo hacemos en VBTF o peróxido de hidrógeno (gas o plasma, depende de lo que tengamos). De la entrada de Matachana, me gustan las figuras que utilizan y que aquí reproduzco, por lo intuitivas que son.
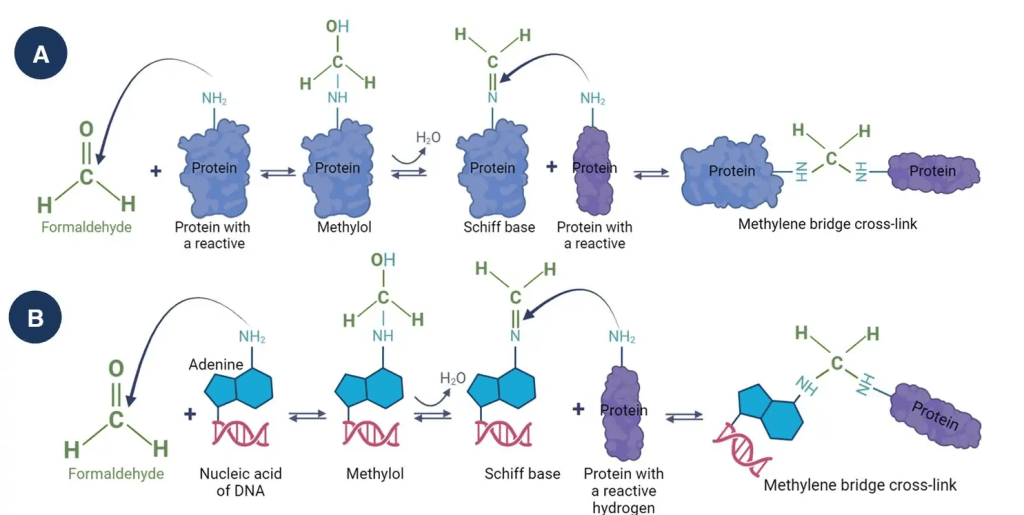
Nos presentan en este trabajo unos resultados obtenidos en su laboratorio (tabla 1) y que habría que reproducir con el peróxido en forma de vapor o gas, ya que en el texto, aunque solo se habla de VH2O2 vaporizado («El Peróxido de Hidrógeno Vaporizado (VH2O2) es una sustancia altamente oxidante»), luego en la tabla parece que se ha usado la forma de peróxido de plasma (se trata de la referencia 14; es del Sterrad, y la 16 es de Steris. La referencia 15 no aparece en el texto- se ha actualizado tras la entrada del blog).
También incidiría en explicar los indicadores biológicos utilizados (se ha actualizado tras la entrada del blog), ya que referencian que usan «La siguiente tabla muestra los resultados de los ensayos de penetrabilidad realizados por el Matachana Test Center, utilizando indicadores biológicos conforme a la norma ISO 11138-5, dentro del receptáculo del PCD con distintas longitudes de trabajo y diámetros internos de lumen». Pero ojo, la UNE-EN ISO 11138-5 es para procesos de esterilización por vapor de agua y formaldehído a baja temperatura, entonces hay que decir la norma para los indicadores biológicos para el peróxido (no he encontrado ninguna norma propia, por lo que supongo que será la UNE-EN ISO 11138-1). Aunque tenemos la norma ISO 11138-6 (en inglés) para esta tecnología.
Tabla 1. Comparación de la eficacia de esterilización entre las tecnologías VH2O2 y VBTF en lúmenes de acero inoxidable (tomado de https://bit.ly/4gF1MRX)
| Diámetro interno [mm] | Longitud [mm] | Esterilización con VBTF Pasa/Fallida | Esterilización con VH2O2 Pasa/Fallida |
| 0,5 | 500 | Pasa | Fallida |
| 1000 | Fallida | Fallida | |
| 0,7 | 500 | Pasa | Pasa |
| 1000 | Pasa | Pasa | |
| 2000 | Pasa | Fallida |
Y sin olvidarnos de los sistemas robóticos que cada día están más presentes en nuestros hospitales, pero cuyos compradores no piensan en que se deben esterilizar.
¿Y qué decir de las lentes de las laparoscopias?
La seguridad y eficacia de cualquier cirugía laparoscópica depende de la claridad de la imagen proporcionada por el sistema de lentes. A pesar de estos avances en óptica, el cirujano sigue padeciendo lentes oscurecidas debido al empañamiento continuo. Tenemos calentadores de lentes o limpiadores de lentes antivaho. La maniobra típica de sacar el laparoscopio, limpiar la lente, aplicar revestimiento antivaho repetidamente y reinserción por la persona de la cámara dentro del abdomen en el momento de la cirugía es realizada repetidamente por los cirujanos, aumentando la duración del acto y uso del bloque quirúrgico, la fatiga, la satisfacción del cirujano y ¿el riesgo de infección? (No está tan claro o no tenemos datos suficientes). Tenemos patente española sobre este tema.
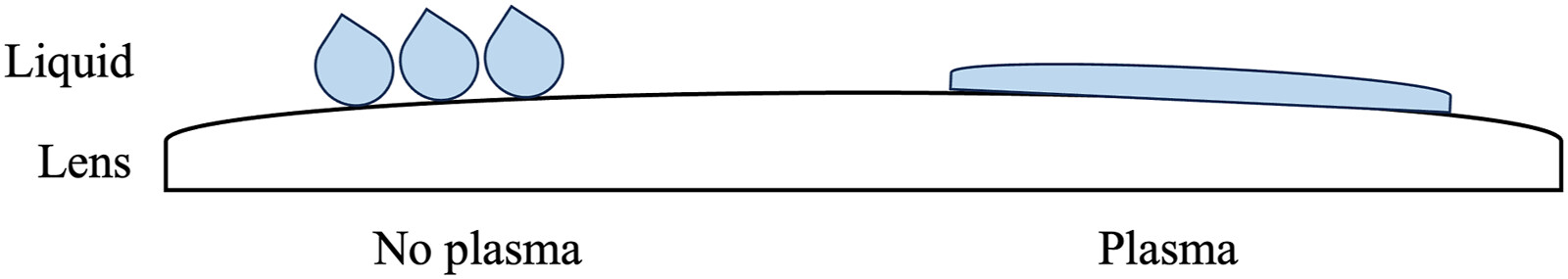
Diversos estudios han identificado las causas del empañamiento de los lentes, principalmente las diferencias de temperatura y la contaminación por fluidos corporales:
- Diferencial de temperatura: El empañamiento se produce cuando la temperatura de la punta del laparoscopio es significativamente inferior a la temperatura de la cavidad abdominal, lo que provoca condensación (Kubo et al., 2022, han observado que una temperatura de la lente inferior a 3,5ºC de la temperatura de la cavidad abdominal produce empañamiento).
- Contaminación: La sangre y los fluidos corporales pueden oscurecer la lente, por lo que es necesario limpiarla con frecuencia, lo que supone una pérdida de valioso tiempo quirúrgico (Rahman et al., 2023, observan un aumento del tiempo operatorio. Hasta el 7,92% del tiempo se dedicó a limpiarlas) (Sekiguchi et al., 2023).
Como sistemas preventivos se propone:
- Calentar el laparoscopio: Calentar la punta del laparoscopio durante al menos diez segundos puede evitar que se empañe al mantener una temperatura cercana a la de la cavidad abdominal (Kubo et al., 2022).
- Métodos de limpieza: Limpiar el cristalino durante 10 a 30 segundos también puede reducir el empañamiento, ya que los tiempos de limpieza prolongados aumentan la probabilidad de que se empañe (Gkegkes & Iavazzo, 2023, que proponen calentar la lente durante al menos diez segundos y limpiando la lente durante 10-30 segundos para mantener una diferencia de temperatura de no más de 3,5 °C en comparación con el abdomen.).
- Diseños innovadores: El desarrollo de lentes superhidrófugos y compresas calientes desechables ha demostrado ser prometedor a la hora de reducir el empañamiento y el tiempo de limpieza durante los procedimientos (Sekiguchi et al., 2023).

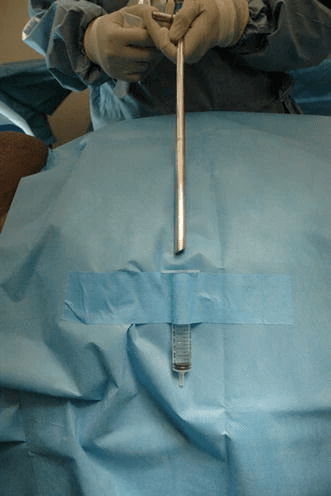
Hay sistemas un tanto artesanales.
No hay un sistema mejor que otro, en esta revisión de 2022, no se encuentran diferencias significativas.
Y como me ha quedado una entrada un poco larga, hoy os dejo dos joyas musicales.
Y aquí algo serio con un bajo de fondo alucinante:














































Debe estar conectado para enviar un comentario.