
En esta entrada vuelvo a tener la colaboración de Bastian Wulff, Responsable de Innovación de la empresa Dr. Weigert.

Para quien no conozca a Bastian, diré que es todo un experto del mundo de la desinfección e higiene. Tengo la suerte de conocerle en persona, después de varios viajes a España, coincidiendo con jornadas y congresos de SEDE y de la WFHSS. La suerte que tenemos con él, es que habla perfectamente el español con un acento gaditano que te sale llamarle «pisha», a lo que hay que unir su cordialidad y humor. Contaré un secreto de él, y es que un gran aficionado al karate y viene a mi ciudad (Talavera de la Reina) a hacer cursos con una de las mejores karatecas del mundo, Sandra Sánchez. Este año, espero contar con él en las II Jornadas de la Sociedad Castellanomanchega de Medicina Preventiva y Salud Pública, que se celebrarán en Cuenca del 18 al 19 de junio.
Ya colaboró en el Blog con una entrada titulada ¿Qué influencia tiene el tiempo de secado en la eliminación de residuos de sangre durante el reprocesamiento de dispositivos médicos? Una investigación a fondo en la que nos detallaba y explicaba un artículo publicado en el Journal Hospital Infection, publicado en el 2025. Esta vez, nos detalla su artículo del año 2026 de la misma revista. Vais a poder leer detalladamente todo el proceso en esta entrada.
Cualquiera que se haya familiarizado con el reprocesamiento de productos sanitarios se dará cuenta rápidamente de lo complejo que es en realidad este tema que, a primera vista, parece sencillo. Hay muchas razones para ello: la gran variedad de tipos de instrumentos quirúrgicos, materiales a reprocesar, máquinas y productos de limpieza, los diferentes tipos y grados de contaminación, los tiempos de reposo del instrumental y muchos otros factores más.
Por eso, en la práctica, se presentan una y otra vez casos en los que algunos instrumentos quirúrgicos no quedan limpios, aunque la razón no sea evidente. Uno de estos casos fue el punto de partida para que nos ocupáramos intensamente del comportamiento de la sangre al secarse.
En Alemania, Suiza y Austria, para la validación y el control del rendimiento de los procesos de limpieza, conforme a la norma ISO 15883-1/-2/-5 y la directriz nacional [1,2], se utilizan pinzas Crile contaminadas con sangre de oveja coagulada. Estas pinzas se pueden adquirir en el mercado o el validador responsable las contamina con sangre de oveja heparinizada y reactivada, de acuerdo con la normativa [2]. Tras la limpieza, se realiza una cuantificación de los residuos proteicos utilizando métodos establecidos, como el método BCA y el método OPA.
Lo último fue el caso cuando un día nos contactó un usuario que nos informó de un aumento inusual en los valores de proteínas residuales durante la revisión del rendimiento de los procesos de limpieza, a pesar de que el resultado del reprocesamiento en la central en cuestión seguía siendo bueno y sin cambios aparentes. Al principio no teníamos ni idea de qué podía estar pasando. Sin embargo, pronto se descubrió que no se habían respetado los tiempos de espera especificados al preparar las pinzas, sino que habían utilizado los instrumentos para las pruebas después de solo una hora de secado a temperatura ambiente. Una prueba rápida en el laboratorio mostró diferencias significativas en el resultado de la limpieza cuando la sangre solo se había secado durante una hora. Esto fue sorprendente, ya que hasta entonces habíamos asumido que los residuos más secos siempre eran más difíciles de eliminar que los relativamente frescos.
Por lo tanto, decidimos investigar sistemáticamente la influencia de diferentes tiempos de secado. En primer lugar, esto se llevó a cabo en forma de contaminación superficial homogénea en placas de acero inoxidable, ya que estas permiten condiciones definidas en el laboratorio y la mejor reproducibilidad posible. Ya informé sobre los resultados de este estudio el año pasado en este blog. Descubrimos que la sangre es especialmente resistente cuando está coagulada, pero aún no se ha secado del todo.[3]
El siguiente paso era verificar estos resultados con instrumentos quirúrgicos reales. Para ello, primero había que resolver un problema: para eluir de forma fiable todos los residuos proteicos de una pinza quirúrgica entera con el propósito de cuantificarlos, se necesita una cantidad relativamente grande de solvente, lo que diluiría mucho las proteínas disueltas y dificultaría su determinación precisa. En particular, los residuos de fibrina, que son especialmente persistentes y representan una proporción relativamente pequeña de la proteína total, podrían pasar desapercibidos. Para evitar este problema, cortamos las articulaciones de los instrumentos y utilizamos solo estas como muestras de ensayo. Las articulaciones, y en particular los residuos que se encuentran dentro de ellas, suponen un desafío especial a la hora de limpiarlas, ya que para el detergente son más difíciles de acceder directamente. Encima, como ya habíamos examinado los residuos de sangre superficiales, decidimos introducir la sangre directamente en la articulación para la nueva serie de experimentos.
Además, simulamos un ciclo de reprocesamiento completo que, aparte del experimento de limpieza realizado en un baño de inmersión, antes de la contaminación con sangre, incluía el tratamiento con un lubricante para el cuidado de instrumentos quirúrgicos y un paso de esterilización a vapor (figura 1).
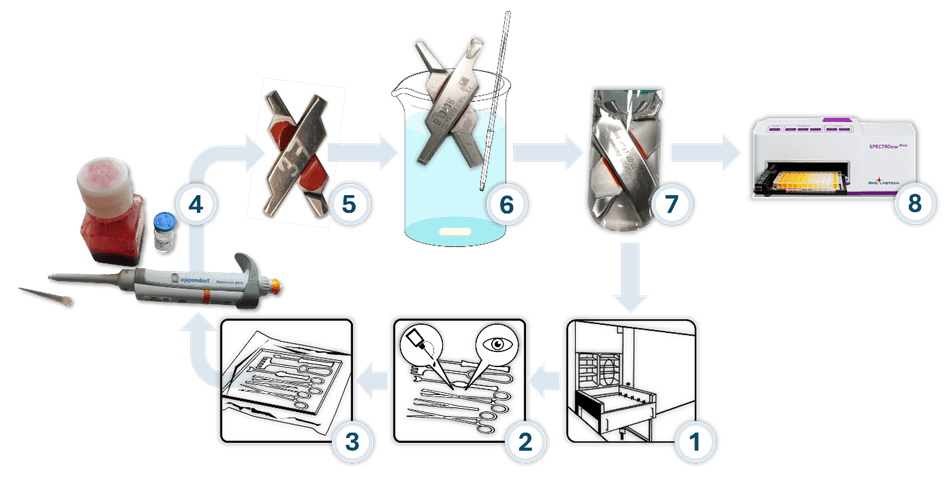
Tanto el paso de limpieza como el cuidado de los instrumentos se llevaron a cabo con dos productos de diferentes fabricantes para poder descartar efectos específicos del respectivo producto. Los residuos de proteínas que quedaron después de la limpieza se determinaron utilizando el método BCA, uno de los procedimientos estándar mencionados en la norma EN ISO 15883-5 para la cuantificación de proteínas residuales. En la figura 2 se muestra un resumen de los resultados de los estudios.
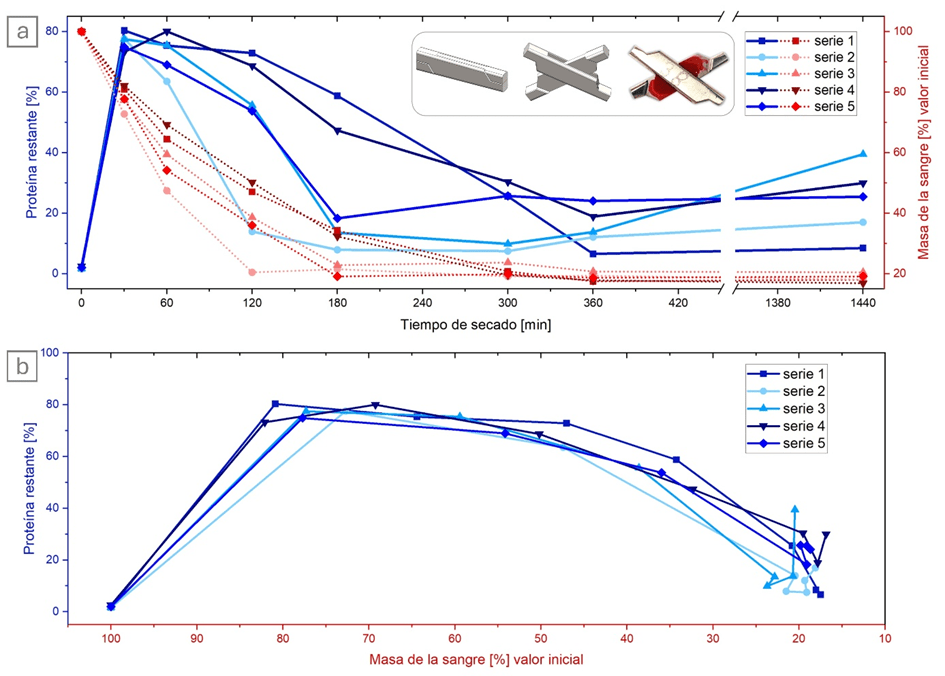
Vemos claramente que la mayoría de los residuos proteicos permanecieron durante las primeras 2-3 horas de secado y que los valores disminuyeron después. Tras un tiempo de reposo más prolongado (24 h), las cantidades de proteína volvieron a aumentar ligeramente (efecto de envejecimiento/fase de maduración). Aunque en esta ocasión la sangre se pipeteó en la articulación de un instrumento y no se distribuyó uniformemente sobre una superficie, se observó exactamente el mismo efecto que habíamos observado y descrito anteriormente.
La representación de la figura 2(b) muestra el efecto independientemente del tiempo y, en su lugar, utiliza la cantidad de proteína en función del progreso del secado. Dado que al secar la sangre se evapora el agua, se puede seguir perfectamente el proceso pesando las muestras.
En resumen, podemos concluir lo siguiente:
- Si la sangre es fresca y aún no ha comenzado a coagularse o la coagulación no ha avanzado mucho, se puede eliminar fácilmente.
- Si la sangre se ha coagulado y aún no se ha secado, es más difícil de eliminar.
- Si la sangre se ha secado, es más fácil de eliminar (siempre que no lleve mucho tiempo).
- Si la sangre seca lleva mucho tiempo secándose, ocurren procesos químicos de envejecimiento que hacen que sea más persistente y difícil de eliminar.
Ahora la pregunta clave es, por supuesto: ¿qué implicaciones concretas tiene esto para la práctica del reprocesamiento de productos sanitarios?
Una aplicación es obvia, ya que fue el motivo que nos llevó a realizar nuestras investigaciones: la validación de procesos y el control del rendimiento de los procesos de limpieza con pinzas contaminadas, tal y como se utilizan en Alemania, Suiza, Austria y, de forma aislada, en otros países como Polonia. En España y Latinoamérica este tipo de práctica de validación (todavía) no es habitual.
Más difícil de determinar es la importancia que esto tiene para la práctica diaria del reprocesamiento. No obstante, intentaremos encontrar una respuesta. Para ello, primero debemos saber en qué fase del secado se encuentran normalmente los instrumentos cuando comienza el reprocesamiento. Aquí ya nos encontramos con la primera dificultad para responder a esta pregunta. Es evidente que existe una enorme variedad. Los tiempos de traslado y de espera dependen de muchos factores. Además de la distancia entre la sala del quirófano, que puede estar justo al lado o ni siquiera en el mismo edificio, por no hablar de los reprocesadores externos, también influyen de manera decisiva, por ejemplo, la organización interna del trabajo, las condiciones de almacenamiento y transporte, la urgencia del reprocesamiento y, por supuesto, el momento de uso del instrumento y la duración de la operación.
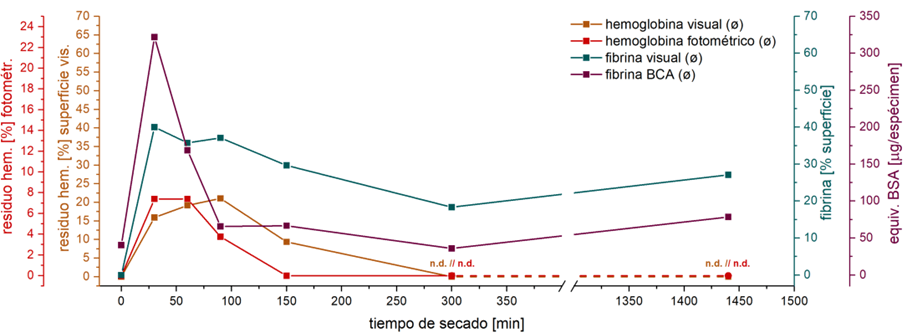
Del estudio de campo con un detergente para el reprocesamiento de productos sanitarios, tengo los datos sobre el tiempo de reposo de los instrumentos antes del procesamiento de siete hospitales diferentes de Alemania. Aunque esta muestra no es para nada representativa, los datos nos dan algunas pistas y nos servirán como base para este experimento mental. Los intervalos de tiempo mencionados van desde unos pocos minutos hasta 72 horas, si los instrumentos en cuestión permanecían sin procesar durante el fin de semana. A primera vista, llaman la atención las grandes diferencias entre los distintos centrales y los intervalos de tiempo, en algunos casos muy amplios. La vista general de la figura 3 muestra, en una superposición gráfica con los datos experimentales del estudio, en qué intervalos de tiempo la sangre sería especialmente resistente según nuestros experimentos.
Los tiempos de secado mencionados no tienen en cuenta el tiempo de uso en el quirófano ni el momento de uso, que son imposibles de determinar con exactitud para cada instrumento individual. Esto da lugar a otro factor con una gran variabilidad temporal. Para algunas de las intervenciones quirúrgicas más frecuentes se dispone de datos sobre la duración típica de la operación. [5] Esta suele oscilar entre 1 y 2,5 horas. Por lo tanto, para nuestro análisis, añadimos 1,5 horas al tiempo de secado para el uso en el quirófano, sabiendo que, debido a la gran variabilidad temporal, solo puede ser una aproximación muy vaga.
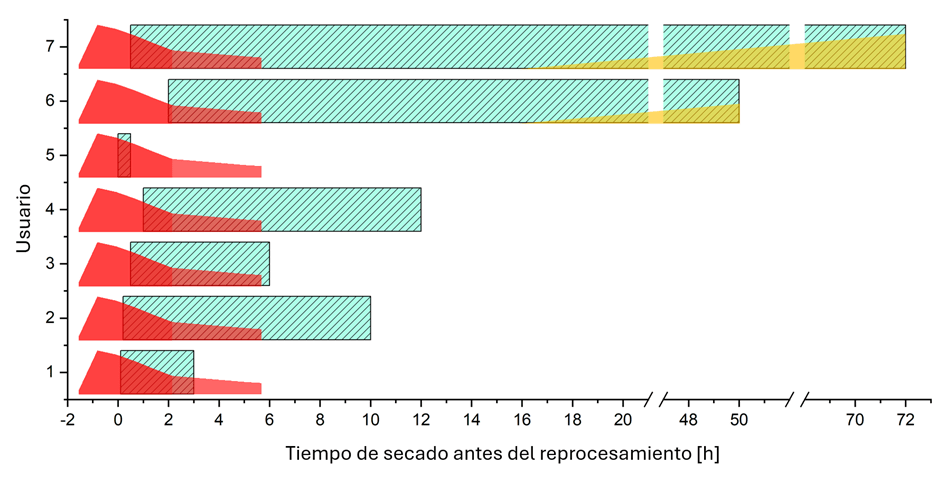
Si echamos ahora un vistazo a la gráfica, podemos afirmar con bastante certeza que, a pesar de todo, siempre habrá instrumentos que se vean afectados por este efecto en mayor o menor medida.
Pero ¿de qué nos sirven exactamente estos conocimientos teniendo en cuenta la enorme variabilidad temporal?
Si los instrumentos presentan anomalías en el resultado de la limpieza sin motivo aparente, la causa podría ser un tiempo de reposo desfavorable antes del procesamiento, especialmente si esto ocurre repetidamente en determinados procedimientos. Estos procesos podrían revisarse de forma específica y, si fuera necesario, ajustarse. En caso de resultados inesperados en el contexto de las evaluaciones de procesos, se recomienda revisar la metodología, en particular el cumplimiento con los tiempos de espera especificados en la preparación de las muestras estandarizadas.
¿Qué puedo hacer para evitar este tipo de problema?
¿Debo dejar mis instrumentos más tiempo sin limpiar? En algunos casos, un tiempo de reposo más largo probablemente tendrá un efecto positivo en el resultado de la limpieza, pero hay que tener en cuenta que un tiempo de reposo más largo también puede dar lugar a otros problemas. Por ejemplo, el contacto prolongado con medios corrosivos como la sangre o los desinfectantes para heridas aumenta el riesgo de daños por corrosión y también afecta al flujo de trabajo de la central de esterilización, ya que retrasa el reprocesamiento. En su lugar, en el caso de instrumentos afectados, el pretratamiento con productos enzimáticos no fijadores de proteínas en el punto de uso puede ofrecer una solución, especialmente si estos productos también tienen buenas propiedades inhibidoras de la corrosión. [6]
¿Qué limitaciones hay?
En la realidad, los instrumentos quirúrgicos no solo están contaminados con sangre, sino que a menudo también con mezclas de sangre, mucosidad, restos de tejido, desinfectantes para heridas o similares. El comportamiento de estas mezclas al secarse puede diferir considerablemente del comportamiento de la sangre pura. Por lo tanto, aunque los resultados de nuestro estudio pueden ayudar a completar el panorama general, solo representan una pieza más del complejo puzle que es el reprocesamiento de los productos sanitarios y no permiten sacar conclusiones absolutas y universalmente válidas sobre el comportamiento de secado de las contaminaciones en el contexto quirúrgico. No obstante, conocimientos como estos nos ayudan de manera significativa en muchos ámbitos, no solo en los ejemplos mencionados, como la práctica de validación, sino también, por ejemplo, en el desarrollo y ensayo de nuevos productos como detergentes y equipos para el reprocesamiento de productos sanitarios.
Referencias bibliográficas
[1] DIN EN ISO 15883-5:2021-11. Washer-disinfectors – Part 1: General requirements, terms and definitions and tests; – Part 2: Requirements and tests for washer-disinfectors employing thermal disinfection for critical and semi-critical medical devices; – Part 5: Performance requirements and test method criteria for demonstrating cleaning efficacy.
[2] Carter A, Eibl R, Krüger S, Gebel J, Niebur S, Hoppe M, et al. Guideline compiled by DGKH, DGSV and AKI for the validation and routine monitoring of automated cleaning and thermal disinfection processes for medical devices 5th edition. Central Service Suppl. 2017.
[5] https://wiki-science.blog/surgery-duration-guide-common-operations (consultado 21/01/2026).
[6] “Folleto rojo” Tratamiento del instrumental – método correcto para el tratamiento del instrumental. Grupo de trabajo Tratamiento del Instrumental (AKI) 11.a edición 2017.
Conclusiones que saco yo:
El estudio revela que la dificultad para limpiar la sangre no aumenta linealmente con el tiempo, sino que sigue un patrón de «montaña rusa» basado en su estado físico:
- Punto de máxima resistencia: La sangre es más difícil de eliminar cuando está coagulada pero aún húmeda, lo que ocurre típicamente entre las 2 y 3 horas de secado.
- La paradoja del secado: Una vez que la sangre se seca completamente, su eliminación es temporalmente más sencilla que en la fase de coagulación húmeda.
- Efecto de envejecimiento: Tras 24 horas, la resistencia vuelve a subir debido a procesos químicos de maduración.
- Implicación en validaciones: El incumplimiento de los tiempos de secado estandarizados en las pruebas de control (como usar pinzas tras solo una hora de secado) genera resultados de proteínas residuales inusualmente altos.
- Recomendación práctica: Dado que muchos instrumentos llegan a limpieza en su fase más crítica, se aconseja el pretratamiento con productos enzimáticos en el punto de uso para evitar la fijación de proteínas y la corrosión.
La eficacia de la limpieza no depende únicamente de que la sangre esté “fresca” o “seca”, sino del momento exacto dentro del proceso de secado. Dado que en la práctica clínica siempre existirán instrumentos expuestos a tiempos de reposo desfavorables, es fundamental considerar este efecto en la validación de procesos, en la interpretación de resultados anómalos y en la organización del reprocesamiento. Medidas como el pretratamiento en el punto de uso con productos adecuados pueden mitigar el problema.
Me despido con música italiana de mi infancia con Monsieur Glisolfi:
Y un pasodoble dedicado a Soria, porque yo lo valgo:







































Debe estar conectado para enviar un comentario.